【概要】
哺乳類を含む全ての多細胞生物は、細胞同士が互いに接着し合って様々な組織や臓器を構成しているが、その細胞同士の接着の強さは一体どれ くらいなのか? 生命科学は今日までに著しく進歩したが、この初歩的とも言える問いに関してはほとんど答えてこなかった。その理由は、個々の細胞が非常に 小さく(径10ミクロンほど)、構造は脆弱であるのに細胞同士の接着が相当に強固であるため、接着している細胞同士を引き離し、その強さを測定することが 困難であったからだ。奈良先端科学技術大学院大学(学長:磯貝彰)物質創成科学研究科の細川陽一郎特任准教授と近畿大学(学長:畑博行)医学部の伊藤彰彦 教授の研究グループは、フェムト秒レーザーと呼ばれる特殊なレーザー発生装置を使い、細胞培養液にレーザー光を当てたとき、その集光点近傍の非常に狭い領 域(径10ミクロンほど)に衝撃波が発生することに着目。この現象を利用して、生体と同様の環境下で細胞同士を引き剥がす細胞操作技術と、レーザー衝撃波 の強さを測定する技術の開発に成功した。この2つの技術を融合させることにより、生体内で細胞同士が接着する力を力学単位で見積もることが可能となった。
当 研究グループは、細胞同士の接着が重要な役割を果たす生命現象として白血球が移動する遊走と上皮細胞同士の強固な接着に注目した。白血球は健常時全身の血 管内を循環しているが、組織の傷害が起こるとその部位において血管壁をすり抜けて血管の外に出てきて、炎症を惹起する。この遊走現象の第一歩は、白血球が 血管内皮細胞に接着することである。一方、上皮細胞は生体の表面に存在して外界との境界を成す組織単位であり、互いに強固に接着して異物の侵入を防いでい る。当研究グループはこれらの接着力をレーザー照射によって力学単位(力積=ニュートンと時間の積)で測定し、後者が前者の約10倍強いことを明らかにし た。本技術により初めて、あらゆる形態をとる生体の細胞間接着を一律の基準で定量化でき、生体内の様々な細胞の営みを統合的に理解する新しい道を拓く。
今 回の技術開発は、医学の分野にも貢献する可能性を秘めている。実際、当研究グループは、神経系と免疫系との細胞間接着力の計測にも成功しており、病的なス トレス応答(喘息やアトピー性皮膚炎)が接着力で説明できるのではないかと研究を進めている。また、白血球の遊走現象は癌細胞の転移現象と類似するので、 転移成立と癌細胞接着力との関係解析から転移の分子メカニズム解明へとつながる可能性が期待される。さらに、再生医学の分野でも、試験管内で発生させた上 皮組織が本来の細胞間接着力を有しているかどうかの検定に有用と考えられる。
本研究成果は高く評価され、平成23年1月18日(火)にアメリカ科学アカデミー紀要(Proceedings of National Academy of Science,U.S.A.)の電子版に掲載されました。
【解説】
こ の測定技術では、光を10兆分の1秒の時間(10―13 秒=100フェムト秒)に集中させたフェムト秒レーザーと呼ばれる超短パルスレーザーが用いられ る。顕微鏡に培養細胞試料を配置し、そこに高強度のフェムト秒レーザーを集光すると、集光点では時間的空間的に集められた超高密度な光エネルギーにより爆 発現象が引き起こされる。ミサイル爆撃では爆発点のみならず、その近傍の構造物も衝撃波により吹き飛ばされる。それと同様に、この場合でも爆発点である集 光点で発生した衝撃波により、集光点近傍にある細胞が吹き飛ばされる。フェムト秒レーザーを用いることにより顕微鏡下でその集光点の大きさを1ミクロン程 度にすることができ、その衝撃波の影響も数10ミクロンの領域のみに制限することができる。細胞の大きさは10ミクロン程度であるのでフェムト秒レーザー は、1細胞を狙って強い衝撃波を付加することのできる極小の誘導ミサイルとして利用できる。さらにレーザー強度を調整することにより、その衝撃波の大きさ を自在にコントロールできる。
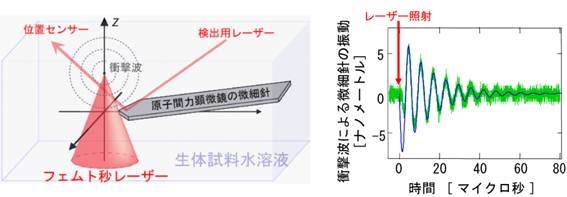
この様な衝撃波の発生については、これまでに知られていたが、その極微空間における衝撃波の大きさを定量する方法が なかった。細胞間の接着力を評価するためには、この衝撃波を定量化する必要があり、細川特任准教授は原子間力顕微鏡を利用してこの衝撃波を定量する新手法 を考案した。原子間力顕微鏡では、幅10ミクロン、長さ100ミクロン程度の微細針の動きをナノメートルの精度で検出することができ、原子や分子の配置を 調べるために用いられている。この微細針をフェムト秒レーザーの集光点近傍に配置し(図1)、衝撃波により誘導される微細針の動きを検出することで、衝撃 波を定量することに成功した。この方法は、原子間力顕微鏡の技術者から「先生、使い方をご存じですか?」と言われるほど奇抜な発想である。原子間力顕微鏡 を壊してしまうことも想定される実験であるにも関わらず、そのチャレンジ精神を評価して支援いただけた科学研究費補助金 若手研究(A)のお陰で、本研究を実行することができた。
微細針により衝撃波を定量した後、培養細胞試料を配置し、標的とした細胞間の接着が引き 剥がされる距離を調べた。培養細胞試料のデザインは伊藤教授らのグループにより行われた。伊藤教授は、実験病理学を専門としており、これまでに病変を構成 する細胞間の細胞接着と情報伝達過程の関わりについて調べ、疾患における病態の形成を分子・細胞レベルで明らかにしてきている。
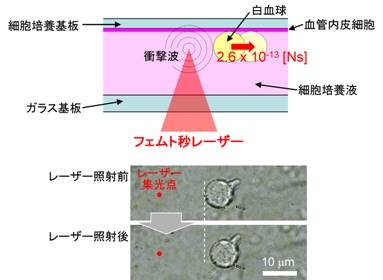
本研究ではまず、血管内皮細胞の上に白血球を配置した試料を用いて実験をおこなった(図2)。この実験により本手法による接着力測定の妥当性が証明され、さらに従来法では評価できない浸潤がすすんだ白血球の接着力も評価できることが示された。
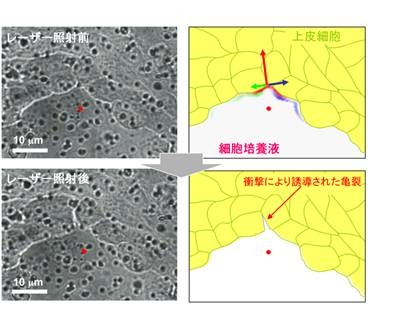
次 に、皮膚を構成する上皮細胞の培養試料を用いて実験を行った(図3)。上皮細胞は、細胞接着分子であるカドヘリンにより互いに強固に接着していることが知 られており、容易にその細胞間の接着を引き剥がすことはできない。興味深いことに、フェムト秒レーザーにより発生した極短時間の強い衝撃波は、細胞の弾性 を無視し、岩を割れ目から裂くように、両者の細胞間の接着を引き裂がされた亀裂が観察された。この結果は、従来方法では細胞同士が強く結びつきすぎて評価 が不可能であった細胞間接着に対しても、本手法が適用できる可能性を示すものである。
このように本研究は、全く専門分野が異なる細川特任准教授と 伊藤教授が、互いの専門性を最大限に引き出しあった結果であり、世界的にみても新規な異分野研究であることは間違いない。さらには両教授に共感し、熱心に 実験と研究を推進した奈良先端科学技術大学院大学物質創成科学研究科博士後期課程1年飯野敬矩氏、東京大学医科学研究所博士課程3年萩山満氏の貢献により 達成された。
今後、動物細胞のみではなく植物細胞に対してもこのレーザー衝撃による非接触計測方法を適用し、植物が外部環境に如何に応答し、その 形態を形成するかを明らかにすることを計画している。さらに本手法の用途は細胞に限定されるものではない。例えば、マイクロマシン(MEMS)中の微小素 子の接合強度評価、生体適合性材料や蛋白質結晶などの脆性材料のマイクロレベルでの強度評価などにも利用できると考えられ、今後の広い応用が期待される。
【用語解説】
「フェムト秒レーザー」
光 を100兆分の1秒の時間(10―14 秒=10フェムト秒)領域に集中させたレーザー。10フェムト秒の時間で、光は3ミクロンしか進むことができな い。300ナノメートルの光が10周期程度しか振幅できない時間であり、フェムト秒以下の時間では光が光である性質がくずれるとされ、光にとっての極限の 時間であると言える。
「原子間力顕微鏡」
幅10ミクロン、長さ100ミクロン程度の微細針の先端に検出用レーザーを導入し、そこ からの反射光を位置センサーにより検出することで(図1参照)、微細針のナノメートルオーダーの動きを、ミクロンオーダーの光位置の変位として検出する装 置で、AFM (Atomic Force Microscope)とも呼ばれる。この微細針の先端には更に、先端をナノメートルオーダーに尖らされた超微細針が接着されており、その針で材料表面を ナノメートルの精度でなぞることにより、そこに存在する原子や分子の形状を直接しらべることができる。本研究では、フェムト秒レーザーにより引き起こされ た衝撃波を、この微細針のナノメートルの振動として検出している。
「細胞接着分子」
細胞の接着を司る蛋白質の総称。接着分子は細 胞膜を貫いて、或いは細胞膜の表面にアンカーして存在し、細胞膜の外側の部分で他の細胞の接着分子や細胞外マトリックス(コラーゲンなどの線維成分)と結 合する。接着分子にはいくつもの種類があり、細胞が移動する際にその方向や速度を決定したり、細胞同士を強く接着させて異物の侵入を防ぐ組織を作ったりし ている。
「血管内皮細胞」
血管の内腔を裏打ちする細胞。一般に平坦な形をしており、血管の内面ではこの細胞が1層敷き詰まってい る。健常状態では内皮細胞の表面は非常に平滑であるが、周囲の組織が損傷されると、細胞表面の接着性が上昇し、血管内を循環する血液細胞(好中球やリンパ 球)の一部が内皮細胞に捕捉される。これが炎症反応の始まりとされる。
「上皮細胞」
多細胞生物において外界との境界面に配列する 細胞の総称。上皮細胞は一般に互いに強固に接着し、全体として精緻な構造物を成す。例えば、皮膚の最表層では、上皮細胞が何層も重なって存在しており、表 皮という強固な組織を構成している。表皮は外界からの異物の侵入に対する防御機構の根幹である。また、消化管や気道粘膜の最表層では上皮細胞が一列に並ん で存在し、種々の酵素を含む粘液を分泌している。
【下図の解説】
図1.原子間力顕微鏡を利用したフェムト秒レーザー衝撃波の計測システム
生 体試料水溶液中にフェムト秒レーザーを集光し、集光点で爆発現象を引き起こすことにより衝撃波を発生させる。原子間力顕微鏡の微細針は、この衝撃波を受け ることで動き出す。この動きを、微細針の先端に導入している検出レーザーの反射光を位置センサーにより検出することで検出する。微細針のバネ定数は既知で あり、レーザー衝撃波による微細針の振動(右図)を解析することで、レーザー集光点(爆発点)で発生した衝撃波の大きさを求めることができる。
図2.フェムト秒レーザー衝撃波による血管内皮細胞に接着した白血球の剥離
基 板上に培養した血管内皮細胞の上に白血球を接着させた試料を用いており、上図のように白血球の側方にフェムト秒レーザーを集光し、衝撃波を発生させ、その 衝撃波により白血球を血管内皮細胞から剥離させた。集光点で発生した衝撃波力の大きさは、白血球の代わりに原子間力顕微鏡の微細針を配置することにより調 べられており、その結果を基に白血球に加わる力が、力積として2.6 x 10-13 [Ns]と見積もられた。下の写真は、フェムト秒レーザーの入射方向から見た白血球の透過顕微写真であり、レーザー照射前後で細胞が移動していることが分 かる。
図3.フェムト秒レーザー衝撃波による上皮細胞間の接着乖離
左側はフェムト秒レーザーの入射方向から見た上皮細胞の透過 顕微鏡写真である。写真に見える多数の黒点は、細胞培養基板の通気孔である。右側は左側の写真に対応する模式図であり、黄色い領域に上皮細胞が存在し、白 い領域には細胞培養液のみが存在する。上側と下側は、それぞれレーザー照射前と後の顕微写真と模式図である。図中赤点はレーザー集光点であり、レーザー照 射後に集光点(爆発点)に近い上皮細胞間に亀裂が誘導された。この集光点で発生した衝撃波の大きさも原子間力顕微鏡により見積もられており、上皮細胞と細 胞培養液の界面には、赤青緑のグラデーションと矢印で示された分布の衝撃波が加わると計算される。矢印の大きさに対応する力積は、赤:13.9 x 10-13 [Ns]、青:8.0 x 10-13 [Ns] 、緑:5.9 x 10-13 [Ns]であり、その接着乖離には、血管内皮細胞-白血球の接着乖離(図2)よりも大きな衝撃波を必要とする。