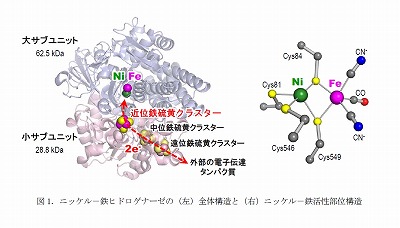
奈良先端科学技術大学院大学(学長:小笠原直毅)物質創成科学研究科の超分子集合体科学研究室廣 田俊教授と太虎林特任助教の研究グループ、兵庫県立大学(学長:清原正義)生命理学研究科の樋口芳樹教授、及び科学技術振興機構(理事長:中村道 治)CRESTの共同研究グループは、水素分子の分解反応や水素分子をつくりだす合成反応を可逆的に触媒する酵素(ニッケル-鉄ヒドロゲナーゼ、図1)に ついて、この酵素に含まれる「鉄硫黄クラスター」といわれる部分がスイッチ役になってこの酵素の触媒反応を制御するメカニズムを初めて明らかにした(図 2、3)。この酵素による水素分子の分解・合成反応は、現在燃料電池等に利用されている白金等の希少金属触媒と比べて高効率で行われており、今回の成果 は、新規の燃料電池や水素合成触媒の開発につながる研究と期待されている。
ヒドロゲナーゼは、微生物が有する酵素で水素分子の分解・合成 を司る。ヒドロゲナーゼはその活性部位の金属錯体の構成金属の違いから3種類に分類され、それぞれニッケル-鉄ヒドロゲナーゼ、鉄-鉄ヒドロゲナーゼ、鉄 ヒドロゲナーゼとよばれる。このうちニッケル-鉄ヒドロゲナーゼは、最もよく研究されてきた酵素で、大小2つのタンパク質(サブユニット)からなり、ニッ ケル-鉄活性部位は大きなサブユニット中にある。触媒反応が起こる時、水素分子の分解・合成によりこのニッケル-鉄活性部位の配位構造は3つの状態をとる (図3)。また、触媒反応に関わる電子は小さなサブユニットにある3つの鉄硫黄クラスターを通って外部のタンパク質分子とやりとりされる(図1)。この酵 素に光を照射すると、ニッケル-鉄活性部位は3つの状態とは異なる新たな状態になることが知られていたが、その状態が触媒反応において意味を持つのかは謎 であった。
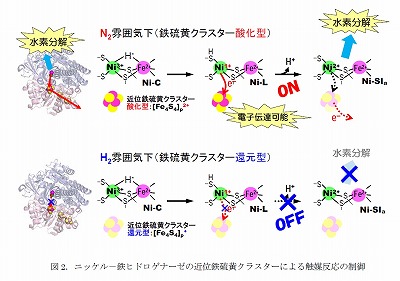
廣田教授らは、フーリエ変換赤外吸収分光法という分子構造を調べる方法を用い、光照射で生じる状態が触媒反応の中間体であるこ とを突き止めた。さらに、3つの鉄硫黄クラスターのうちニッケル-鉄活性部位に最も近いクラスターの電子状態を調べた結果、そのクラスターが還元されてい る時は触媒反応が進まず、酸化されている時だけ進むことを見出した(図2)。つまり、活性部位に最も近い鉄硫黄クラスターがスイッチ役になってヒドロゲ ナーゼの反応を制御していることを明らかにした。
この成果は、10月9日(木)にオンライン発行されたドイツの「Angewandte Chemie International Edition(アンゲバンテ・ケミー・インターナショナル・エディション」に掲載されました。
水 素分子は究極のクリーンエネルギーとして、その利用に向けた基礎および応用研究が急がれてきた。微生物由来であるヒドロゲナーゼは、水素分子の分解・合成 反応を常温常圧で触媒することから、その分子システムの理解はバイオ電池およびその活性部位を模倣した新規の水素合成触媒や人工燃料電池の開発につながる と期待されている。ヒドロゲナーゼの高効率な触媒反応のしくみを理解するためには、酵素のニッケル-鉄活性部位で起こる反応機構の解明が不可欠である。こ れまでの様々な研究により、水素分子の分解・合成が行われるニッケル-鉄活性部位の情報は蓄積されてきたが、反応により供給・放出される電子を伝達する鉄 硫黄クラスターが酵素活性に及ぼす影響については詳しく調べられてこなかった。
本研究により、3つの鉄硫黄クラスターのうち、ニッケル- 鉄活性部位の最も近くにある「近位の鉄硫黄クラスター」が触媒反応を進める時のスイッチ役となり、このクラスターの酸化状態によりヒドロゲナーゼの活性が 制御されることが明らかとなった。本研究は、新規の水素合成触媒や燃料電池の開発につながる研究と期待されている。
【解説】
ニッ ケル-鉄ヒドロゲナーゼの活性部位のニッケル原子には、硫黄(S)原子を含んだ4つの「システイン」と呼ばれるアミノ酸残基が結合(配位結合)し、それら のうち2つは鉄原子にも配位し、ニッケルと鉄の橋渡しになる構造を形成している(図1)。さらに、鉄原子には1個の一酸化炭素(CO)と2個のシアン化物 イオン(CN-)も配位している。
一方、小さなサブユニットには、ニッケル-鉄活性部位からの距離が異なる、3つの鉄硫黄クラスター(近 位鉄硫黄クラスター([Fe4S4]p2+/+)、中位鉄硫黄クラスター([Fe3S4]m+/0)、遠位鉄硫黄クラスター([Fe4S4]d2+ /+))が配置され、ニッケル-鉄活性部位の水素分解過程で生じる電子を外部の電子伝達タンパク質へ伝達する(図1)。
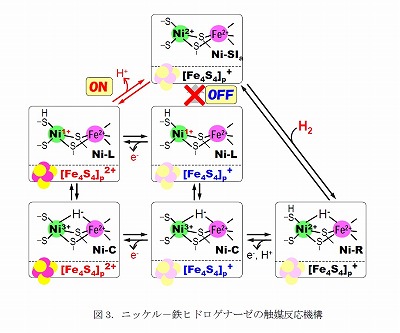
ニッケル-鉄ヒドロゲナーゼでは、ニッケル-鉄活性部位の配位構造の違いにより、Ni-SIa、Ni-R、Ni-C型と呼ばれる3つの状態を順に形成して、水素分子を分解する(水素分子を合成するときはNi-SIa、Ni-C、Ni-R型の順に形成)。
廣田教授、太特任助教、樋口教授らは、このようなニッケル-鉄ヒドロゲナーゼの触媒反応を近位鉄硫黄クラスターが制御する機構を明らかにした(図2、3)。
ま ず、分子の構造がわかる「フーリエ変換赤外吸収分光法(FT-IR)」という手法を用い、レーザー光(波長514.5 ナノメートル)を照射した際の分子の構造変化を調べた。水素や窒素を含む環境で鉄硫黄クラスターの酸化状態を変え、-135℃~-75℃でFT-IRスペ クトルを測定することにより、光により生成する「Ni-L型」といわれる構造が「Ni-C型」と 「Ni-SIa型」間で構造が変化する際の中間体であることを発見した。次いで、電子状態がわかる「電子スピン共鳴分光法(EPR)」という手法を用い、 近位鉄硫黄クラスターが酸化されている時のみNi-C型からNi-SIa型構造への変換が行われることを見出した。
実験では、 -135℃~-75℃で水素か窒素を含む環境下で、光照射時と光照射前のフーリエ変換赤外吸収スペクトル(FT-IRスペクトル)の比較からニッケル-鉄 活性部位の構造変化を調べ、「Ni-C型」が「Ni-L型」構造を介して「Ni-SIa型」構造へ変換することを初めて特定した。さらに、温度を上げて反 応を活発にすると「Ni-C型」から「Ni-SIa型」構造への変換率が上昇することからも、「Ni-L型」構造が反応中間体であることが確かめられた。
ま た、「電子常磁性共鳴分光法(EPR)」の実験では、「Ni-C型」構造を取った場合の「近位鉄硫黄クラスター」の酸化還元の状態を調べ、水素がある環境 下では、ほとんどすべて還元されるのに対して、窒素がある環境下では約15%が酸化されていることがわかった。Ni-C型構造における「酸化されている」 近位鉄硫黄クラスターの割合は、「Ni-C型」から「Ni-SIa型」構造への変換率(約14 %)とよく一致しており、Ni-C型からNi-SIa型構造への変換は、近位鉄硫黄クラスターが「酸化されている」ときにのみ起こることが明らかになった (図2)。
つまり、「Ni-L型」から「Ni-SIa型」構造への変換の祭、1個の電子がニッケル-鉄活性部位から放出され、近位鉄硫黄 クラスターへ流れると考えられる。窒素がある環境下では、一部の近位鉄硫黄クラスターは酸化されており、電子を受取ることができる。しかし、水素がある環 境下では、ほとんど全ての近位鉄硫黄クラスターは還元されており、電子数が最大に達しているため電子を受け取れず、Ni-L型はNi-SIa型構造へ変換 されない。
こうしたことから、近位鉄硫黄クラスターが水素分解・合成反応を進めるかどうかのスイッチ役になっており、近位鉄硫黄クラスターの酸化還元の状態によりヒドロゲナーゼの活性が制御されることを明らかにした。
【研究の位置づけ】
水 素分子は究極のクリーンエネルギーとしてその利用に向けた基礎および応用研究が急がれてきた。ヒドロゲナーゼは水素分子の分解・合成反応を常温常圧で触媒 することから、その分子システムの理解はバイオ電池およびその活性部位を模倣した新規の人工燃料電池や水素合成触媒の開発につながると期待されている。ヒ ドロゲナーゼの高効率な触媒反応のしくみを理解するためには、酵素のニッケル-鉄活性部位で起こる反応機構の解明が不可欠である。これまでの様々な研究に より、水素分子の分解・合成が行われるニッケル-鉄活性部位の情報は蓄積されてきたが、反応により供給・放出される電子を伝達する鉄硫黄クラスターが酵素 活性に及ぼす影響については詳しく調べられてこなかった。
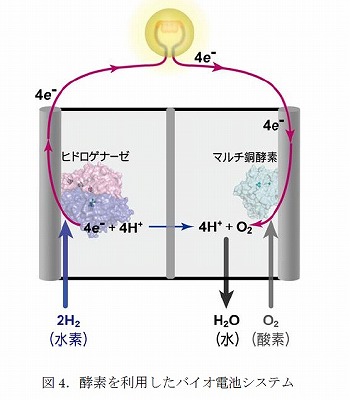
本研究により、鉄硫黄クラスターが水素分解・合成反応のスイッチ役となってお り、近位鉄硫黄クラスターの酸化還元の状態によりヒドロゲナーゼの活性が制御されることが明らかとなった。本酵素のニッケル-鉄活性部位における、水素分 子の分解・合成の反応がどのように進行していくかが詳しく分かってきたことで、今後、人工触媒系の設計に寄与できる情報が増えた(図4)。また、本メカニ ズムは水素分解・合成を行う化合物合成にも有用な情報となる。
本研究成果は、科学技術振興機構(JST)戦略的創造研究推進事業 チーム型研究(CREST)「ライフサイエンスの革新を目指した構造生命科学と先端的基盤技術」研究領域(研究総括:田中啓二)における研究課題「生物酵 素による水素エネルギー利用システムの構造基盤解明」により得られました。
【用語解説】
①「フーリエ変換赤外吸収分光法(FT-IR)」
赤 外吸収分光法は、分子の振動による赤外線吸収を測定することで、分子構造の情報を得る振動分光法の1つである。干渉計を用いたフーリエ変換赤外吸収分光法 は波数精度が極めて高く、近年広く使用されている。観測される振動数は、分子内の結合の強さに鋭敏であり、反応種の状態を特定するときにも用いられる。 ニッケル-鉄ヒドロゲナーゼでは、鉄原子に結合した1つの一酸化炭素(CO)と2つのシアン化物イオン(CN-)に由来するバンドがそれぞれ、 1880~1970 cm-1に1つ、2040~2110 cm-1に2つ観測され、これらのバンドの振動数より、ヒドロゲナーゼの状態を特定することができる。
②「電子常磁性共鳴分光法(EPR)」
マ イクロ波を用いて不対電子(原子の最外殻の軌道で対になっていない電子)を検出する手法。磁場の影響下に置かれた試料中の不対電子は、ある特定のエネル ギーを持つマイクロ波を共鳴吸収し、高いエネルギー準位へと遷移する。鉄硫黄クラスターのうち、鉄原子4つ、硫黄原子4つからなる鉄硫黄クラスター ([Fe4S4] 2+/+)では還元型がEPR活性であるのに対して、鉄原子3つ、硫黄原子4つからなる鉄硫黄クラスター([Fe3S4] +/0)では酸化型がEPR活性である。
【関連リンク】
・タイトル
Control of the Transition between Ni-C and Ni-SIa States by the Redox State of the Proximal Fe[BOND]S Cluster in the Catalytic Cycle of [NiFe] Hydrogenase
・論文は以下に掲載されております。
http://dx.doi.org/10.1002/anie.201408552
・以下は論文の書誌情報です。
Dr. Hulin Tai, Dr. Koji Nishikawa, Dr. Masayuki Suzuki, Prof. Dr. Yoshiki Higuchi and Prof. Dr. Shun Hirota
Angewandte Chemie International Edition, Article first published online:8 OCT 2014